اين شاخه از فيزيك به مطالعه گرما و حركت، روابط بين گرما و انرژي مكانيكي، الكتريكي و ساير انواع انرژي يا كار ميپردازد. ترموديناميك مبحثي مشترك بين شيمي و فيزيك است كه در كتاب سال سوم شيمي هم درباره آن مطالبي را ميخوانيد.
در ترموديناميك دستهاي از مولكولها را از بقيه مولكولها جدا كرده و يا جدا در نظر ميگيرند و سپس به بررسي آنها
ميپردازند. اصطلاحاً اين مولكولهاي جدا شده يا جدا در نظر گرفته را سيستم يا دستگاه (System) مينامند. به فضاي اطراف سيستم، محيط (Surroundings) گفته ميشود.
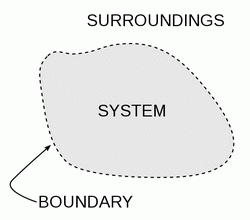
سيستم توسط مرزي از محيط جدا ميشود.
از نظر سير تاريخي هم ترموديناميك سهم بسيار مهمي در انقلاب صنعتي داشته است. ماشينهاي بخار كه گرما را به انرژي مكانيكي تبديل مينمودند، به سرعت جايگزين نيروي انساني در كارگاهها، كارخانهها، معادن، حمل و نقل،
كشتيراني و مزارع كشاورزي شدند. توماس سيوري، توماس نيوكامن و جيمز وات سازنده و تكميل كننده اولين ماشينهاي بخار بودند.





 پاسخ با نقل قول
پاسخ با نقل قول










علاقه مندی ها (Bookmarks)